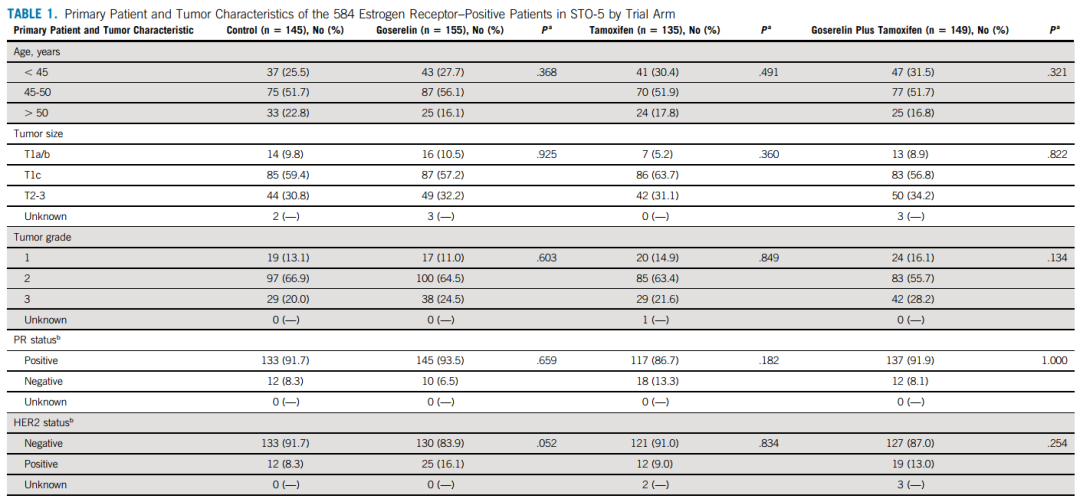
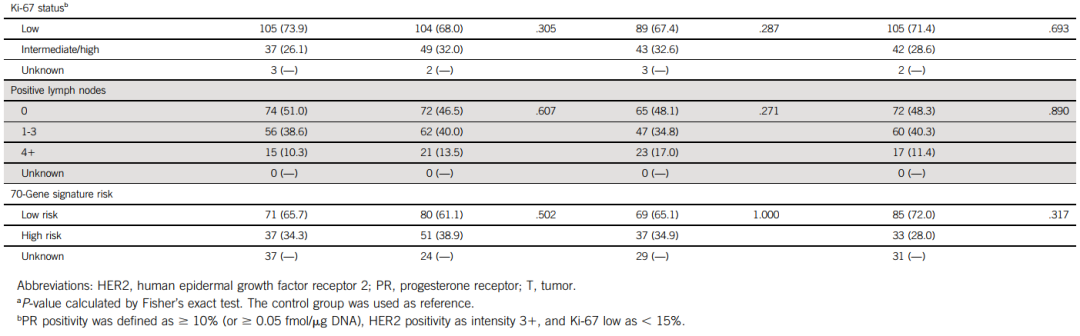
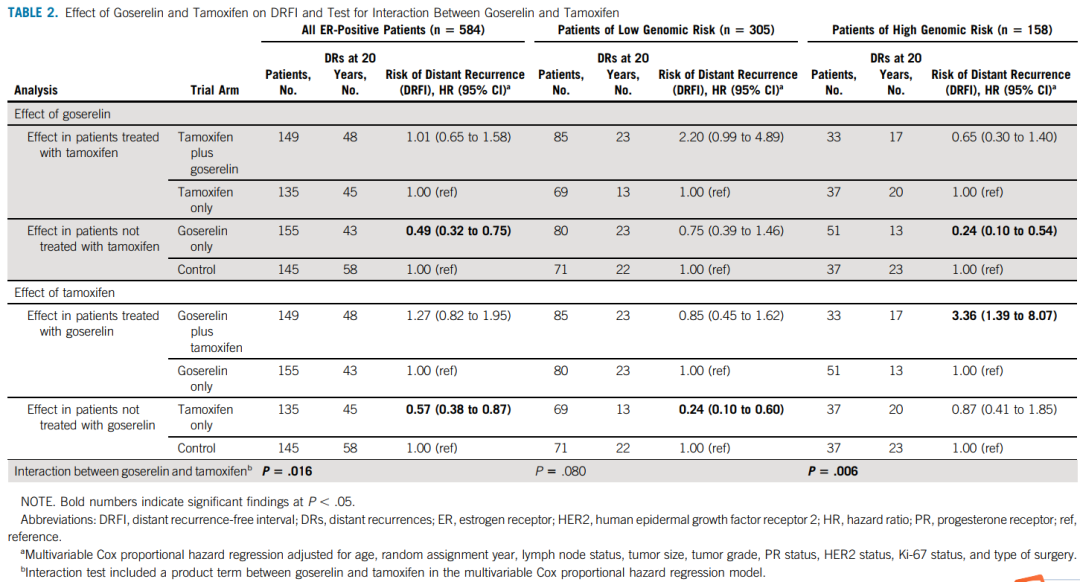
评估绝经前乳腺癌患者长期(20年)内分泌治疗的获益。 方法 斯德哥尔摩试验 (STO-5,1990-1997)将924例绝经前患者随机分配至2年戈舍瑞林(3.6 mg皮下注射,每28天一次)、Tamoxifen/ target=_blank class=infotextkey>他莫昔芬(40 mg口服,每日一次)、戈舍瑞林和Tamoxifen/ target=_blank class=infotextkey>他莫昔芬联合治疗组或无辅助内分泌治疗组(对照组)。随机分配按淋巴结状态分层;淋巴结阳性患者 (n = 459) 被分配至标准化疗组(环磷酰胺、甲氨蝶呤和氟尿嘧啶)。2020年进行了原发性肿瘤免疫组织化学 (n = 731) 和基因表达谱分析 (n = 586)。70个基因标记确定了基因组低风险和高风险患者。Kaplan-Meier分析、多变量 Cox 比例风险回归和多变量时变灵活参数模型评估了长期无远处复发间期 (DRFI)。随访20年。 结果 在雌激素受体阳性患者(n = 584,中位年龄47岁)中,与对照组相比,戈舍瑞林、他莫昔芬和联合治疗显著改善了长期无远处复发间期(多变量风险比 [HR],0.49;95%CI,0.32至0.75,HR,0.57;95%CI,0.38至0.87,HR,0.63;95%CI,0.42至0.94)。观察到显著的戈舍瑞林-他莫昔芬相互作用 (P = .016)。基因组低风险患者 (n = 305) 从他莫昔芬显著获益(HR,0.24;95%CI,0.10至0.60),基因组高危患者(n = 158) 从戈舍瑞林显著获益(HR,0.24;95%CI,0.10至0.54)。在基因组高危患者中观察到在戈舍瑞林基础上加用他莫昔芬的风险增加(HR,3.36;95%CI,1.39至8.07)。而且,在基因组低风险患者中观察到持久的20年他莫昔芬获益,而基因组高风险患者具有早期戈舍瑞林获益。 结论 这项研究显示,在雌激素受体阳性的绝经前患者中,辅助内分泌治疗2年可使20年获益,并根据肿瘤基因组特征提示不同的治疗获益。戈舍瑞林和他莫昔芬联合治疗与单药治疗相比无获益。评估治疗获益的长期随访至关重要。 引言 绝经前乳腺癌患者发生致死性疾病的风险增加。由于这些患者在早期被诊断,因此长期风险和治疗获益在该患者组中尤其值得关注。绝经前雌激素受体 (ER) 阳性乳腺癌的标准辅助治疗是他莫昔芬治疗5年或以上。对于高风险疾病(通常由标准临床标志物定义,包括淋巴结受累、高肿瘤分级、高增殖、高基因组风险标记评分和年龄低于40岁),建议使用其他卵巢功能抑制 (OFS),如促黄体激素释放激素激动剂戈舍瑞林和/或化疗。因此,尽管临床医生越来越倾向于推荐OFS,但尚不清楚哪些患者应接受该治疗。 背景:SOFT的结果表明,在他莫昔芬基础上加用 OFS 可显著改善绝经前患者的生存率,中位随访时间相对较短,为8年。然而,仅将 OFS 随机分配不包括在 SOFT 中,并且由于患者入组是在21世纪初,因此不可能随机分配至未治疗组。此外,亚组分析得出的结论是,在一组年龄稍小(中位年龄40岁)、既往化疗后恢复绝经前状态的临床高危患者中观察到他莫昔芬和 OFS 联合治疗的主要效应。与 SOFT 相反,绝经前患者的 Zoladex(ZIPP) 试验表明,戈舍瑞林和他莫昔芬联合治疗并不优于任一单药治疗模式。联合治疗并不优于单药治疗似乎存在争议,但在绝经后患者的Arimidex、他莫昔芬单药或联合治疗 (ATAC) 研究中也观察到了这一点,其中芳香化酶抑制剂和他莫昔芬联合治疗与芳香化酶抑制剂单药治疗相比并未改善生存期。ZIPP试验 (STO-5) 的斯德哥尔摩部分的优势在于,患者被严格随机分配至4个试验组,因此,STO-5试验也进行了单独分析。此外,由于在试验开始时尚未明确确定绝经前内分泌治疗的获益,STO-5试验纳入随机分配至无辅助内分泌治疗组。因此,这项四组试验现在能够结合来自高质量瑞典登记研究的独特长期随访,对内分泌治疗与对照进行独特的评估。 大量证据表明,ER阳性乳腺癌患者发生远处转移复发的长期风险稳定,其中大部分事件发生在初次诊断后10年以上。鉴于此,需要更长时间的随访来了解 ER 阳性乳腺癌患者的真正内分泌治疗获益。此外,辅助 OFS 治疗的长期获益仍未知,因为普遍缺乏10年或10年以上结局数据的临床试验。STO-5试验目前已经完成了20年的随访;介绍了长期内分泌治疗对绝经前乳腺癌患者的益处,这些患者被随机分配接受两年的戈舍瑞林、他莫昔芬、两者联合或不辅助内分泌治疗。此外,使用分子70基因标记风险预测工具,根据基因组风险分层评估治疗组特异性内分泌治疗的获益。该标记在年轻乳腺癌患者中具有已知的预后效用,但其是否具有内分泌治疗预测价值仍未探索。 方法 患者:1990年5月至1997年1月,斯德哥尔摩试验(STO-5)入组了924例诊断为浸润性可手术乳腺癌的绝经前患者。随机分配包括4个试验组:2年戈舍瑞林(3.6 mg皮下注射,每28天一次)、他莫昔芬(40 mg口服,每日一次)、戈舍瑞林和他莫昔芬联合治疗或无辅助内分泌治疗(对照)。根据患者的淋巴结状态将随机分配分为三组;0、1-3和4个或更多阳性淋巴结(图1)。在内分泌治疗的同时,淋巴结阳性患者接受标准辅助化疗(环磷酰胺、甲氨蝶呤和氟尿嘧啶)。有4个或4个以上阳性淋巴结的患者接受局部放疗;详情见数据补充。 图1.STO-5 试验的CONSORT 图。 a731例患者进行了免疫组化评估。CMF,环磷酰胺、甲氨蝶呤和氟尿嘧啶;ER,雌激素受体;RT,放疗 免疫组织化学 2020年,与卡罗林斯卡大学医院病理科合作,按照标准化临床方案对ER、孕激素受体 (PR)、人表皮生长因子受体 2(HER2) 和增殖标志物 Ki-67 进行了免疫组织化学 (IHC) 分析;详见数据补充。对731例有可用的原发性肿瘤福尔马林固定石蜡包埋块和足够的侵袭性肿瘤细胞进行分析。731例患者子集的患者和肿瘤特征分布与最初入组的924例患者相似(数据补充)。由有经验的乳腺癌病理学家对每种标志物阳性的癌细胞百分比进行评分。根据瑞典国家指南, ER 阳性和 PR 阳性状态定义为阈值≥10%,Ki-67分为低 (< 15%) 和中/高 (≥15%)。HER2阳性定义为 IHC 强度为3 +。根据该方法确定 IHC 数据缺失但有可用免疫测定34,35(n = 4) 患者的 ER 状态和 PR 状态。共有584例患者患有 ER 阳性肿瘤(图1)。 肿瘤大小和肿瘤分级:根据临床指南将肿瘤大小 (T) 分为3组:T1a/b(≤10 mm)、T1c(11-20 mm) 和T2-T3(> 20 mm)。根据诺丁汉组织学评分系统(Elston分级)进行肿瘤分级。 70-基因风险分类 安捷伦微阵列基因表达谱分析于2019-2021年进行,并使用70个基因标记将原发性肿瘤分为低或高基因组风险。总共有586个肿瘤通过了70个基因标记质量检查,其中463个为ER 阳性(图1)。 结果 STO-5 试验中584例 ER 阳性患者的患者和肿瘤特征在4个试验组之间平衡良好(表1)。中位年龄为47(范围26-55)岁,大多数患者患有2级 (63%)、PR阳性 (91%)、HER2阴性 (88%) 和 Ki-67 低 (70%) 肿瘤。根据试验方案,淋巴结阳性患者 (n = 301,51%) 接受了化疗。 表1.按试验组列出的 STO-5 中584例雌激素受体阳性患者的原发性患者和肿瘤特征 试验组的长期内分泌治疗获益 随机分配至戈舍瑞林组、他莫昔芬组、联合组或对照组的患者经 DRFI 检测的20年生存比例分别为71.6%、66.0%、67.1%和59.7%。单变量 Kaplan-Meier 分析显示,与对照组相比,戈舍瑞林显著改善了长期DRFI(对数秩P = .026,图2A)。在他莫昔芬或联合治疗的单变量分析中,未观察到长期 DRFI 的显著差异(图 2B 和2C)。多变量 Cox 比例风险回归分析显示,与对照组相比,戈舍瑞林、他莫昔芬和联合治疗显著改善了长期DRFI(风险比 [HR],0.49;95%CI,0.32至0.75,HR,0.57;95%CI,0.38至0.87,HR,0.63;95%CI,0.42至0.94)(图2)。校正年龄、随机分配年份和淋巴结状态的粗分析产生了相似的估计值。 图2.随机分配接受2年 (A) 戈舍瑞林、(B) 他莫昔芬、(C)戈舍瑞林和他莫昔芬联合治疗的患者与随机分配未接受辅助内分泌治疗的患者(对照)比较,DRFI的 Kaplan-Meier 和多变量 Cox 比例风险回归分析。 多变量分析还评估了戈舍瑞林在接受或未接受他莫昔芬治疗的患者中的作用,反之亦然。与他莫昔芬单药或戈舍瑞林单药相比,未观察到戈舍瑞林和他莫昔芬联合给药的显著长期获益(表2)。此外,观察到戈舍瑞林和他莫昔芬之间存在显著相互作用 (P = .016)。 表2.戈舍瑞林和他莫昔芬对 DRFI 的影响以及戈舍瑞林和他莫昔芬之间相互作用的检测 按基因组风险分层的长期内分泌治疗获益 在463例可获得70个基因标记风险分类的 ER 阳性患者肿瘤样本中进一步评估了长期内分泌治疗获益(图3)。肿瘤分类为超低风险的患者数量较少 (n = 51),无法进行有意义的分析。基因组高危患者 (n = 158) 更有可能年龄更小和淋巴结阳性,肿瘤体积更大、分级更高、PR阴性状态、HER2阳性状态和Ki-67 水平更高。尽管如此,分别有60%和47%的基因组高危和低危患者为淋巴结阳性,37%的基因组高危患者为 Ki-67 低。 (A-C) Patients of low genomic risk and (D-F) patients of high genomic risk. 图3.随机分配接受2年戈舍瑞林、他莫昔芬以及戈舍瑞林和他莫昔芬联合治疗的患者与随机分配至无辅助内分泌治疗(对照)的患者比较,DRFI的 Kaplan-Meier 和多变量 Cox 比例风险回归分析,按基因组风险分层。 分层单变量 Kaplan-Meier 分析(图3)显示,与对照组相比,他莫昔芬组基因组低风险患者的长期 DRFI 无显著改善(对数秩P = 0.137,图3B),但戈舍瑞林组基因组高风险患者的长期 DRFI 显著改善(对数秩P < 0.001,图3D)。值得注意的是,在 Kaplan-Meier 图中,早期观察到基因组高危患者中 DRFI 与戈舍瑞林的差异,而基因组低危患者中他莫昔芬的差异在约10年后首次观察到(图 3B 和3D)。此外,分层多变量分析显示,基因组低风险患者他莫昔芬 (HR,0.24;95%CI,0.10-0.60) 和基因组高风险患者戈舍瑞林(HR,0.24;95%CI,0.10-0.54;图3)显著改善长期DRFI。粗分析产生了相似的结果。试验组和基因组风险组的患者和肿瘤特征没有显著差异,尽管与对照组相比,在基因组低风险他莫昔芬治疗患者中观察到年龄略小。 与任一单药治疗相比,进一步的多变量分析显示,在基因组低风险或高风险患者中,联合治疗无显著长期获益。然而,在基因组高危患者中,观察到在戈舍瑞林基础上加用他莫昔芬后远处复发的长期风险显著增加(HR,3.36;95%CI,1.39至8.07)。戈舍瑞林和他莫昔芬之间的相互作用在基因组高危患者中显著 (P = 0.006) ,但在基因组低危患者中不显著 (P = 0.080)。 内分泌治疗获益的时变分析 进行了随时间变化的多变量分析,以评估远处复发风险和治疗获益如何随时间变化。在既往分析中观察到显著和潜在的时变效应后,该分析重点关注基因组低风险患者中的他莫昔芬和基因组高风险患者中的戈舍瑞林。 基因组低风险患者具有稳定的远处复发长期风险。估计的风险率从第5年至第10年略微增加,并在整个20年随访期间保持稳定。此外,与对照组相比,从第4年至第20年观察到他莫昔芬的长期获益,第5、10、15和20年的 HR 显著估计显示风险降低(第20年HR,0.23;95%CI,0.06-0.92;表3)。 表3.DRFI的时变分析 基因组高危患者早期风险,早期获益于戈舍瑞林。在前5年内观察到风险率大幅增加,此后迅速下降。与对照组相比,在前8年观察到戈舍瑞林组的 DRFI 显著改善,第5年的统计学显著估计 HR 为0.26(95%CI,0.11至0.61)(表3)。 讨论 对照随机化研究中,对 ER 阳性乳腺癌绝经前患者进行的这项研究表明,与无辅助内分泌治疗相比,戈舍瑞林、他莫昔芬和联合治疗2年可显著获益20年。此外,这项研究表明,基因组低风险患者从他莫昔芬中具有显著的持久获益,而基因组高危患者从戈舍瑞林中具有早期获益。戈舍瑞林和他莫昔芬联合治疗与单药治疗相比未显示长期获益。STO-5试验的优势包括长期高质量随访和纳入随机分配至无内分泌治疗的对照组患者。 ER阳性患者在初次诊断后几十年远处复发和致死性转移性疾病的风险保持稳定。因此,对这些患者进行长期随访对于了解真正的治疗获益至关重要。影响晚期复发的机制仍不明确,但可能涉及休眠的低增殖肿瘤细胞,其转移生长会被不确定的微环境或全身刺激唤醒,导致增殖-凋亡平衡后期向有利于转移增殖的方向转变。 STO-5 试验中的基因组低风险患者具有稳定的长期远处复发风险,而基因组高风险患者具有较高的早期风险,这证明了绝经前 ER 阳性患者中的异质性转移潜力。观察到的不同治疗获益表明,ER激动剂/拮抗剂他莫昔芬治疗2年可更有效地预防基因组低风险患者的晚期复发,而戈舍瑞林治疗2年(诱导全身雌激素快速耗竭)可最有效地降低更具侵袭性的基因组高危肿瘤的早期风险。这些发现强调了 ER 阳性乳腺癌生物学异质性的临床重要性,并证明需要根据预后和预测肿瘤特征个性化绝经前辅助内分泌治疗。 如今,建议临床高危患者在他莫昔芬的基础上加用OFS,通常定义为淋巴结受累、高级别、高增殖、高基因组风险评分或年龄低于40岁。然而,确定患者的风险具有挑战性,且研究之间存在差异。例如,SOFT使用包括不同肿瘤特征的 Cox 模型测量的连续复合风险,而风险分类是通过 MINDACT 试验中不同肿瘤特征的组合进行。在这里,我们使用70个基因标记评估了患者的基因组风险。正如预期的那样,高基因组风险在更大程度上与更具侵袭性的肿瘤特征相关,如肿瘤体积更大、分级更高和 HER2 阳性状态,但也存在明显的患者间异质性。值得注意的是,大约40%的基因组高危患者患有淋巴结阴性疾病或低增生性肿瘤。此外,根据 MINDACT 定义, 22%的STO-5 基因组高危患者临床风险较低。显然,需要更好地了解风险,尤其是长期风险(超过5-10年)在很大程度上尚未探索,绝经前和绝经后患者之间的风险定义很可能不同。 STO-5 试验观察到与单药治疗相比,戈舍瑞林和他莫昔芬联合治疗没有获益,也表明戈舍瑞林和他莫昔芬之间存在显著的相互作用。相比之下,与他莫昔芬单药相比,SOFT显示 OFS 和他莫昔芬联合治疗改善了无病生存期和总生存期,但未改善远处复发率。值得注意的是,SOFT中未纳入仅随机分配至 OFS 组,因此,无法评估 OFS 和他莫昔芬之间的相互作用。此外,联合治疗的获益主要见于既往化疗后恢复绝经前状态的年轻临床高危患者。SOFT的长期随访将证明联合治疗与他莫昔芬单药治疗相比是否有显著的长期获益。与我们的研究相似,在 SOFT 中,未观察到在他莫昔芬基础上加用 OFS 可改善临床定义的低风险患者的生存期。此外,在2007年的荟萃分析和 ZIPP 试验的随访研究中,未观察到在他莫昔芬基础上加用戈舍瑞林可显著降低复发风险。 戈舍瑞林和他莫昔芬如何在机制水平上单独或联合发挥作用,目前尚不完全清楚。简言之,对戈舍瑞林的初始反应是下丘脑促性腺激素释放激素释放增加。然而,在几周内,会发生脱敏作用,并抑制卵巢雌激素的产生,导致绝经后循环雌激素水平升高。另一方面,他莫昔芬作为混合激动剂/拮抗剂,当与乳腺癌 ER 结合时,会改变其转录活性和增殖相关基因的表达。在包括正常子宫内膜在内的一些组织中,他莫昔芬主要作为 ER 激动剂,解释了其与子宫内膜癌的相关性。鉴于作用机制的差异,我们推测当他莫昔芬和戈舍瑞林联合给药时,他莫昔芬的激动作用可能抵消戈舍瑞林的雌激素耗竭作用。与此一致,ATAC试验表明,他莫昔芬的 ER 激动特性可能抵消阿那曲唑在绝经后患者中同时撤除雌激素水平。 STO-5 试验中的患者接受了2年的辅助内分泌治疗,但如今的标准治疗为5年或更长时间。考虑到与戈舍瑞林相关的强烈但可逆的副作用,观察到的2年戈舍瑞林效应可能对无法接受或耐受5年治疗的患者具有临床意义。然而,需要进一步研究以了解2年和5年治疗之间的潜在差异。关于他莫昔芬,很难将 STO-5 试验中 40 mg 每日一次给药2年与 20 mg 每日一次给药至少5年进行直接比较。尚未确定绝经前患者内分泌治疗的最佳剂量和持续时间,可能与绝经后患者不同。 本研究存在局限性。在 STO-5 试验的 ER 阳性子集中,样本量是一个局限性,在解释时应谨慎。由于样本量,进一步的亚组分析(例如,年龄)在统计学上不合理。与当今的治疗方法相当,STO-5试验设计将化疗分配给淋巴结阳性患者。由于试验设计,在 STO-5 试验中无法探索化疗的额外效应。然而,值得注意的是,分别有60%和47%的基因组高危和低危患者为淋巴结阳性并接受化疗。考虑到独特的试验设计和高质量瑞典登记研究的长期随访,本研究的结果与其他试验的结果一起考虑非常重要。重要的是,其他关于辅助内分泌治疗(包括OFS)的研究均未完成超过10年的随访,也未纳入随机分配至无内分泌治疗组或仅随机分配至戈舍瑞林组的对照组患者。 总之,随访20年的 STO-5 试验结果表明,ER阳性绝经前患者接受2年辅助内分泌治疗可获得长期获益。此外,在长期复发风险稳定的基因组低风险患者中观察到他莫昔芬的长期获益,而早期风险的基因组高危患者从戈舍瑞林中获益。对于无法耐受5年内分泌治疗的患者,本研究中观察到的2年治疗的显著获益可能对患者和临床医生均有帮助。然而,还需要进一步的研究来了解最佳治疗持续时间。此外,在 STO-5 试验中未观察到戈舍瑞林-他莫昔芬联合治疗相对于单药治疗的长期获益。 文章总结: 关键目的 考虑到雌激素受体 (ER) 阳性疾病远处复发的长期风险,了解人生早期诊断的绝经前乳腺癌患者的长期内分泌治疗获益非常重要。STO-5 试验完成了20年的随访,将绝经前患者随机分配到辅助戈舍瑞林、他莫昔芬、联合戈舍瑞林-他莫昔芬治疗组或无内分泌治疗组(对照组)。首次评估了戈舍瑞林和他莫昔芬对绝经前患者的长期获益。 生成的知识 这项研究证明了 ER 阳性绝经前患者辅助内分泌治疗2年的长期获益。此外,它表明他莫昔芬在具有长期复发风险的基因组低风险患者中具有持久获益,而基因组高风险患者具有早期风险并从戈舍瑞林中获益。 相关性 绝经前 ER 阳性乳腺癌患者接受内分泌治疗可获得长期获益;然而,异质性转移潜能导致治疗获益存在差异,需要接受个体化内分泌治疗。 内容来源:https://ascopubs.org/doi/full/10.1200/JCO.21.02844
目的