
 药品简介:
药品简介:
百泽安(替雷利珠单抗注射液)是一款人源化 lgG4 抗程序性死亡受体 1(PD-1)单克隆抗体,替雷利珠单抗具有区别于传统PD-1抗体的独特结合表位,通过基因工程改造,替雷利珠单抗可避免与FcγR结合,从而消除了抗体依赖的细胞介导的吞噬作用(ADCP),避免了因T细胞数量减少而影响抗肿瘤疗效,这使得替雷利珠单抗的抗肿瘤活性更高。百泽安是第一款由百济神州的免疫肿瘤生物平台研发的药物,目前正进行单药及联合疗法临床试验,开发一系列针对实体瘤和血液肿瘤的广泛适应症。
是否医保:医保
...|更多产品信息
 科普答疑
科普答疑 上市信息
上市信息


国内上市 一线治疗 替雷利珠单抗(百泽安)PD-1一线治疗鳞状非小细胞肺癌获批上市!





国内上市 一线治疗 替雷利珠单抗中国获批一线治疗肿瘤表达PD-L1的晚期或转移性胃癌或胃食管结


国内上市 一线治疗 百济神州抗PD-1抗体替雷利珠单抗获批用于转移性鼻咽癌患者一线治疗

国内上市 一线治疗 百济神州PD-1抑制剂替雷利珠单抗食管鳞状细胞癌的一线治疗适应症获批!


国内上市 二线治疗 国产PD-1替雷利珠单抗获批上市,治疗复发或难治性经典型霍奇金淋巴瘤

国内上市 二线治疗 国产PD-1替雷利珠单抗获批上市,治疗复发或难治性经典型霍奇金淋巴瘤

国内上市 二线治疗 替雷利珠单抗成为我国首个获批尿路上皮癌适应症的PD-1单抗
 最新研究
最新研究















二线治疗 OS 生存期 “肝”霖初降丨中国原研替雷利珠单抗治疗肝细胞癌关键性研究数据正式亮相ES















 治疗案例
治疗案例


















抗癌故事 60次免疫治疗!把他的好运传递下去!

抗癌故事 当时只道是寻常:差点失去,才学会珍惜
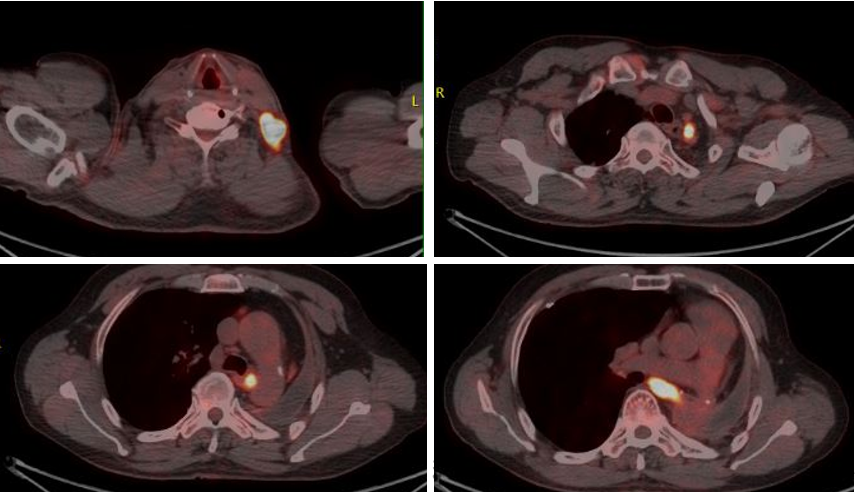

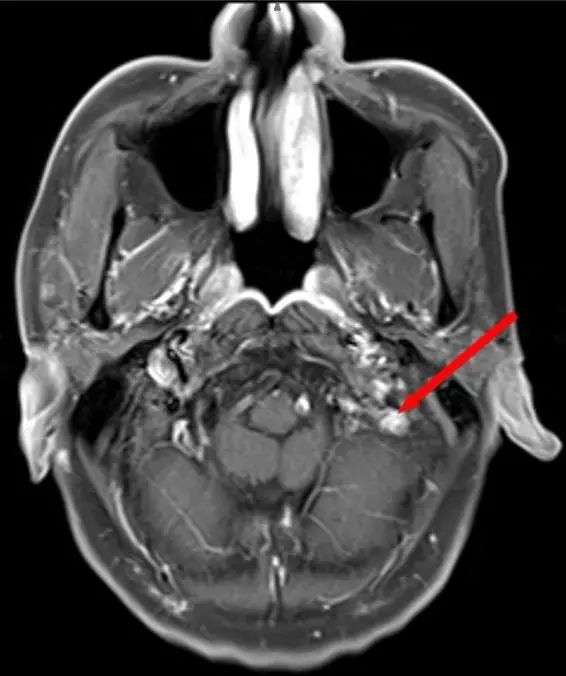



抗癌故事 与死神较量,晚期肝癌也能赢得漂亮!

抗癌故事 肝癌晚期治疗4个月后,肿瘤缩小了一大半




抗癌故事 跨越生死,免疫联合治疗让爱人重获新生













RATIONALE 001研究(NCT02407990)是替雷利珠单抗首个在人体开展的临床试验,纳入了来自澳大利亚、韩国、新西兰和中国等多个国家和地区的27个中心、共451例患者,通过ⅠA/ⅠB期设计充分验证了替雷利珠单抗单药治疗晚期实体瘤良好的安全性/耐受性,以及稳定的药代动力学特性,提供了替雷利珠单抗200 mg剂量依据,并在多种晚期实体瘤患者中观察到疾病缓解。研究数据于2020年6月发表于Journal for ImmunoTherapy of Cancer杂志 进入专栏

RATIONALE 001研究(NCT02407990)是替雷利珠单抗首个在人体开展的临床试验,纳入了来 ... 更多
Ⅱ期
开放标签
多中心
RATIONALE102是一项多中心、开放标签、Ⅰ/Ⅱ期研究,RATIONALE102研究为替雷利珠单抗在中国晚期实体瘤患者中进行的剂量递增和适应症扩展研究。剂量验证阶段确认了替雷利珠单抗的RP2D为200mg, Q3W,未出现剂量限制性毒性(DLT)。治疗第一年内,患者每9周接受一次肿瘤评估(增强CT或MRI),治疗一年后每12周接受一次肿瘤评估(RECIST v1.1),VENTANA PD?L1 (SP263)用于检测肿瘤细胞PD-L1表达水平,PD-L1阳性(PD-L1+)定义为肿瘤细胞PD-L1 进入专栏

Ⅱ期 开放标签 多中心 RATIONALE102是一项多中心、开放标签、Ⅰ/Ⅱ期研究,RATIONALE102研究为替雷利珠单 ... 更多
多中心
RATIONALE 302 研究是一项随机、开放、多中心的全球 3 期临床试验(NCT03430843),旨在评估对比研究者选择的化疗,百泽安?用于治疗既往接受过全身疗法的晚期不可切除或转移性 ESCC 患者的有效性和安全性。 该试验的主要终点为在 ITT 人群中的 OS。试验在横跨亚洲、欧洲和北美的11个国家中入组了 512 例患者,以 1:1 的比例随机至百泽安?试验臂或化疗试验臂(用药选择包括研究者选择的紫杉醇、多西他赛或伊利替康)。 进入专栏

多中心 RATIONALE 302 研究是一项随机、开放、多中心的全球 3 期临床试验(NCT03430843),旨在 ... 更多
Ⅱ期
多中心
RATIONALE 208研究是一项全球、多中心、II期研究(NCT03419897),旨在评价替雷利珠单抗用于二线及二线以上治疗不可切除肝细胞癌患者的有效性和安全性。研究同时纳入接受过一线全身治疗和接受过二线及以上全身治疗的肝细胞癌患者,以替雷利珠单抗200mg IV Q3W方案给药,主要研究终点为独立评估委员会(IRC)评估的ORR,次要研究终点包括研究者(INV)评估的客观缓解率(ORR),IRC和INV评估的疾病缓解持续时间(DoR)、无进展生存(PFS)、疾病控制率(DCR)、临床获益率(CBR 进入专栏

Ⅱ期 多中心 RATIONALE 208研究是一项全球、多中心、II期研究(NCT03419897),旨在评价替雷利珠单抗 ... 更多
一线治疗
RATIONALE-309研究(NCT03924986)旨在评估替雷利珠单抗(抗PD-1抗体)联合GP化疗(吉西他滨和顺铂)对比单独使用GP化疗一线治疗复发或转移鼻咽癌的疗效和安全性。该研究共纳入263例患者,按1:1随机分入A、B两组进行不同治疗,在疾病进展后,经研究者评估仍适合接受免疫治疗的患者,替雷利珠单抗组可继续接受治疗,安慰剂组可以交叉接受替雷利珠单抗单药治疗,中位随访时间15.5个月,主要研究终点为无进展生存期,次要研究终点包括二线无进展生存期、总生存期、安全性等。 进入专栏

一线治疗 RATIONALE-309研究(NCT03924986)旨在评估替雷利珠单抗(抗PD-1抗体)联合GP化疗(吉西他 ... 更多
一线治疗
替雷利珠单抗联合含铂类化疗方案(BGB-A317-206研究)一线治疗中国晚期非小细胞肺癌(NSCLC)和小细胞肺癌(SCLC)试验中,纳入的患者全部为中国人群,旨在研究单抗联合化疗对患者的疗效和安全性.非鳞状非小细胞肺癌患者采用替雷利珠单抗联合培美曲塞与铂类双药化疗四个周期,然后使用培美曲塞进行维持治疗;鳞状非小细胞肺癌患者分别使用替雷利珠单抗联合紫杉醇与铂类的双药化疗(作为A队列)和吉西他滨与铂类的双药化疗(作为B队列);小细胞肺癌的患者采用替雷利珠单抗联合依托泊苷与铂类的双药化疗。 进入专栏

一线治疗 替雷利珠单抗联合含铂类化疗方案(BGB-A317-206研究)一线治疗中国晚期非小细胞肺癌(NS ... 更多
Ⅲ期
Ⅱ期
新辅助治疗
双盲
RATIONALE 315是一项在可切除的II期或IIIA期非小细胞肺癌(NSCLC)患者中比较替雷利珠单抗或安慰剂联合含铂双药化疗作为新辅助治疗,随后接受手术,后续以替雷利珠单抗或安慰剂作为辅助治疗的有效性和安全性的随机、双盲、安慰剂对照的3期临床试验。RATIONALE 315的主要终点为BIPR评估的MPR和BICR评估的EFS。关键次要终点为pCR。其他次要终点包括总生存期(OS)、客观缓解率(ORR)、BICR评估的无病生存期(DFS)和研究者评估的EFS。这一试验共入组453例患者,以1:1的 进入专栏

Ⅲ期 Ⅱ期 新辅助治疗 双盲 RATIONALE 315是一项在可切除的II期或IIIA期非小细胞肺癌(NSCLC)患者中比较替雷利珠 ... 更多