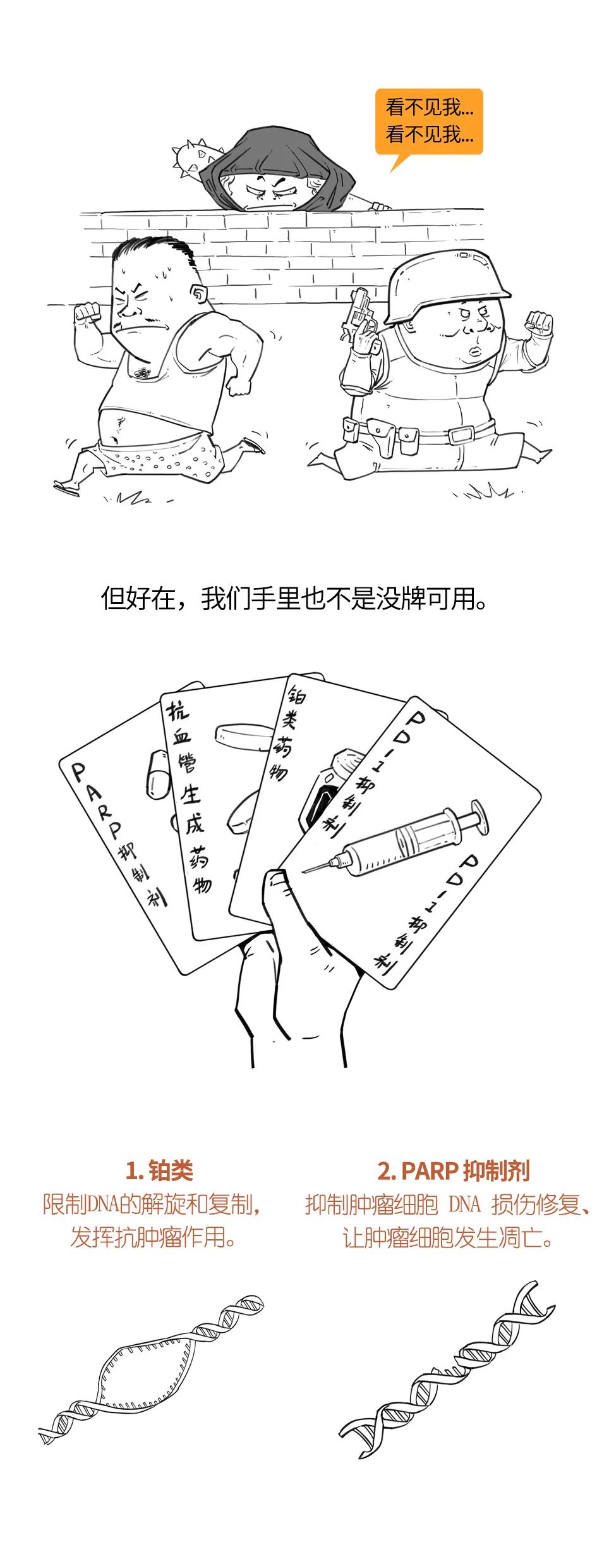
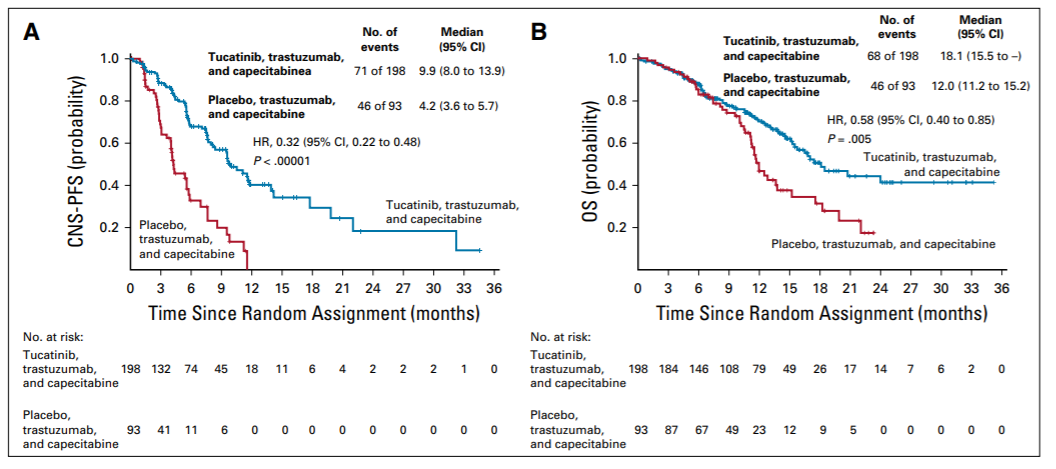
既往,辅助治疗决策多依赖于肿瘤分期、复发转移临床危险度和肿瘤分子分型。
多基因检测(Multigene profiling assays)目前被认为具有「辅助临床决策」的重要作用,可更有利于平衡辅助治疗所带来的疗效与不利,在避免过度治疗、有害治疗方面,具有较好的价值,患者可因此具有更大生存和生活质量的获益。
浙江省医师协会乳腺肿瘤专委会专门就此专题进行投票讨论,并形成初步共识,主要包括21基因检测工具(如Oncotype DX®)、70基因检测工具(Mammaprint®)和28基因检测工具(RecurIndex®)等。
-
如区域淋巴结阴性,推荐可进行21基因检测指导术后辅助系统治疗;
-
如淋巴结1-3枚转移,需谨慎选择21基因检测指导术后辅助系统治疗;
-
RS≥31分,预测均为基因高风险,建议不能豁免化疗;
-
RS<11分,被认为是最保守阈值(远处转移<4%),可较安全豁免化疗;
-
RS 11-25分,整体复发风险仍然较低,通常可豁免化疗。其中对于年龄50岁、RS 16-25分者个体化考虑化疗的必要性;
-
RS 26-30分,尚无明确结果支持豁免化疗的安全性,建议应考虑化疗必要性;
● 研究一:NSABP B-14
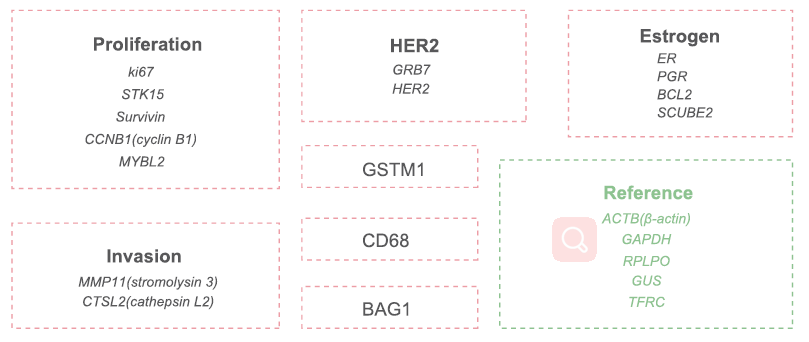
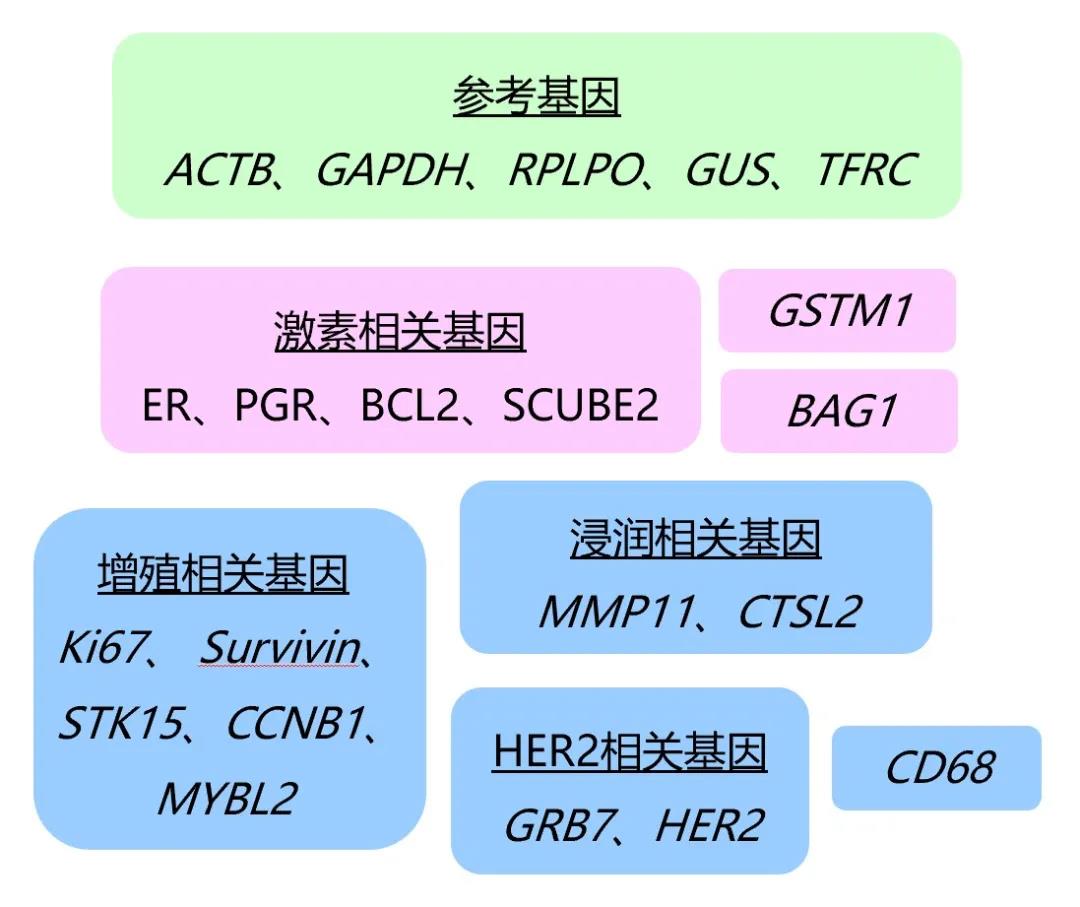
21基因从NSABP B-14临床试验中668例ER阳性、淋巴结阴性患者组织蜡块标本的250个候选基因中,筛选出与远处转移相关的21个基因。
并且,通过基因表达程度、建立分值0-100的复发风险评分标准(RS)和计算公式。
当时RS三分类(<18,≥18<31,≥31)所对应的10年远处转移风险分别为6.8%、14.3%和30.5%;相较于年龄和肿瘤大小,RS为独立预后因素。
● 研究二:TAILORx
TAILORx临床试验对RS进行重新分类和相对应的治疗,关键点分析显示:RS 11-25分组中,单独使用内分泌治疗的患者9年无病生存率与联合化疗组相似(83.3% vs 84.3%)
进一步分析显示,该组中50岁者若为临床低风险,9年远处转移率为4.7%(±1.0%),若为临床高风险,单纯内分泌治疗9年远处转移率超过10%(12.3%±2.4%),而该组大于50岁患者辅助化疗可能过度。
● 研究三:SWOG S8814
SWOG S8814研究纳入的是367例HR阳性HER2阴性、1-3枚淋巴结转移的乳腺癌患者,对于仅接受Tamoxifen/ target=_blank class=infotextkey>他莫昔芬内分泌治疗人群中,RS有预后价值,调整阳性淋巴结个数后,低危组(RS<18)未显示化疗获益。Plan B研究中15.3%的病例(N0-1)RS评分在11分以下,仅接受内分泌治疗的5年DFS可达94%。
这些结果将21基因的应用范围扩大到腋窝淋巴结阳性者(1-3枚)。
但鉴于对于低危阈值界限的不确定性和前瞻性研究RxPONDER结果尚未出炉,目前对于21基因在「淋巴结阳性」人群中的应用NCCN指南作2A类推荐,临床使用仍然需谨慎对待。
-
如具有临床高危特征(比如Adjuvant!Online或基于MINDACT研究的简易风险度分类),可推荐70基因检测指导术后辅助系统治疗;
-
可推荐70基因检测指导术后辅助系统治疗;
-
仅行前哨淋巴结活检且1-2枚转移者(无腋窝清扫状态)进行多基因检测辅助决策需非常谨慎;
-
进行70基因检测需慎重,其作用仅限于可能预测复发风险(20%左右为基因低风险且预后较好);
-
在部分老年、或合并心脏基础疾病、或小肿瘤(T1a)的HER2阳性患者,可作为一种治疗减法的参考,但尚没有数据支持可直接用于术后临床治疗决策;
-
经乳腺癌复发风险28基因检测为低风险的患者,不管后续有无化疗,其10年无远处转移率都较高风险组患者低。